Todos aqueles que já precisaram realizar algum tipo de pesquisa na área de Saúde que envolvesse seres humanos sabe como é complexo e cheio de burocracias. Aprovação em comitê de ética, termo de consentimento assinado pelo paciente, termo de confidencialidade e outras tantas exigências, tudo foi criado com o objetivo de proteger os pacientes. Nem sempre foi assim. Houve uma época em que pesquisas clínicas eram feitas com muito menos exigências em relação à bioética, à segurança ou à privacidade dos pacientes. O que fez com que isso mudasse foi um dos episódios mais vergonhosos da História da Medicina. Um experimento tão infame que se tornou desde então o maior exemplo de como NÃO se fazer um estudo clínico. Um experimento que pretendia estudar os efeitos de uma doença em particular: a sífilis.
Sir William Osler certa vez definiu a sífilis como "a grande imitadora", pela sua capacidade de causar um número enorme de sintomas e mimetizar outras doenças, e isso provavelmente tem a ver com o tipo de lesão que ela causa no organismo. Ela é causada por um tipo muito particular de bactéria, chamada Treponema pallidum, que possui o formato de um saca-rolhas (chamamos as bactérias com essa morfologia de espiroquetas) e com um revestimento que a torna capaz de escapar de boa parte da resposta imune do hospedeiro. Além disso, até hoje ninguém conseguiu fazê-la crescer em uma placa de cultura - o que costuma ser bastante fácil para outros tipos de bactéria - e por esse motivo até o surgimento de técnicas modernas de análise de DNA pouca coisa se sabia sobre os treponemas.
Basicamente, o que a sífilis causa no organismo é uma inflamação na parede dos vasos sanguíneos e nos tecidos em volta. Como temos vasos no corpo todo, essa inflamação pode se espalhar por várias áreas, incluindo a pele e o sistema nervoso. No entanto, parece que os treponemas possuem algum tipo de aversão a altas temperaturas, por isso geralmente a sífilis não costuma acometer as vísceras abdominais.
Didaticamente, dividimos a evolução da doença em três fases. Uma vez que o indivíduo entra em contato com o treponema (a via de transmissão, na grande maioria das vezes, é sexual), os treponemas se espalham por todo o corpo, penetrando até mesmo no líquido cefalorraquidiano entre as meninges, de onde geralmente (mas nem sempre) é eliminado pouco depois. Cerca de 3 a 6 semanas após a infecção, surge uma lesão no local onde o micro-organismo foi inoculado e atravessou a pele ou mucosa - geralmente no órgão genital, mas ocasionalmente no ânus ou na boca. O cancro, como a lesão é chamada, é geralmente uma ulceração indolor, de cor avermelhada e cheia de pequenos treponemas, sendo por isso altamente infecciosa. Essa é o que chamamos de sífilis primária, a primeira fase da doença. Por ser indolor, muitas vezes o cancro passa despercebido, especialmente nas mulheres, e cicatriza poucas semanas depois.
Após um período variável que pode chegar a até mais de 2 meses depois do desaparecimento do cancro, os treponemas espalhados pelo corpo deflagram uma reação inflamatória que constitui a sífilis secundária e se caracteriza por pequenas manchas vermelhas em todo o corpo, parecidas com catapora ou sarampo, mas que têm um diferencial importante: ao contrário dessas outras doenças, na sífilis as manchas vermelhas costumam estar presentes também nas palmas das mãos e nas plantas dos pés. Esse fato ajuda na suspeita diagnóstica da sífilis e é um lembrete sobre por que nós médicos devemos examinar os pacientes com cuidado e atenção. Outras formas de lesão de pele são possíveis, inclusive queda de cabelo em alguns pontos do couro cabeludo e dos supercílios. Como há grande circulação de treponemas, nessa fase também há um nível muito alto de anticorpos contra sífilis circulando no sangue.
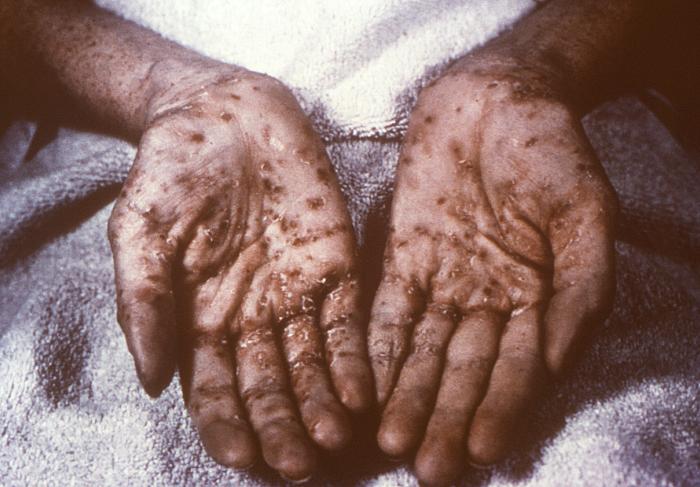
Sífilis secundária acometendo palmas das mãos.
Em alguns dias ou semanas as manchas desaparecem e a doença entra em um estado de latência, na qual pode permanecer silenciosa por muitos e muitos anos ou mesmo para o resto da vida. Mas em alguns casos, dez, vinte ou trinta anos depois, a reação inflamatória causada pelos treponemas pode causar outros problemas, que são conhecidos como sífilis terciária. Tumorações podem surgir em todo o corpo, verdadeiros abscessos chamados de gomas sifilíticas que podem ser desfigurantes ou, se ocorrerem dentro do cérebro, fatais. A inflamação na parede da aorta, a artéria mais calibrosa do corpo e que sai direto do coração, pode deixá-la menos resistente e dar origem a uma dilatação anômala, que chamamos de aneurisma. Sua ruptura pode ser desastrosa, mas felizmente há técnicas cirúrgicas capazes de evitar que isso aconteça se o aneurisma for detectado precocemente. E finalmente há os danos no sistema nervoso, que conhecemos como neurossífilis. Os sintomas podem se assemelhar aos de uma meningite, aos de um AVE, aos de alterações oftalmológicas ou mesmo aos de mania, esquizofrenia ou depressão. Na verdade, a neurossífilis pode mimetizar absolutamente qualquer síndrome neurológica ou psiquiátrica! Inclusive, diante de um idoso com demência, a neurossífilis é uma das causas tratáveis que devem ser excluídas (juntamente com hipotireoidismo e deficiência de vitamina B12) antes de se bater o martelo e afirmar que o paciente tem Alzheimer. À primeira vista, pode ser difícil acreditar que aquele vovô de quase 90 anos pode ter sífilis, mas como a forma terciária pode levar décadas para se manifestar, a investigação de sífilis é sim recomendada.
Existem diferentes formas de se diagnosticar sífilis. O cancro duro, a lesão da sífilis primária, é repleto de treponemas, e basta encostar uma lâmina de vidro sobre a lesão após uma limpeza local, adicionar uma gota de soro fisiológico e levar a um microscópio de campo escuro. Os treponemas são muito pequenos e finos para ser vistos sob técnicas convencionais de microscopia, mas ao microscópio de campo escuro, sob uma luz oblíqua, é possível ver muitos pequenos pontos brilhantes pulando em um fundo negro.
Imagem de treponemas em campo escuro (não se iludam, geralmente a imagem no mundo real não é tão bonita assim)
Talvez a forma mais simples e mais conhecida de se realizar o diagnóstico laboratorial de sífilis seja através do Venereal Disease Research Laboratory test (VDRL). Ele consiste em adicionar uma gota do fluido do paciente a ser testado (usualmente plasma ou líquido cefalorraquidiano) a um extrato de coração de boi, que contém um fosfolipídio chamado difosfatidil-glicerol que também está presente na parede dos treponemas. Caso o paciente tenha anticorpos contra sífilis circulando, eles formarão um aglomerado com o difosfatidil-glicerol que pode ser visto como um precipitado ao microscópio óptico (devido a essa afinidade com o difosfatidil-glicerol do coração bovino, esses anticorpos também são chamados de anticorpos anti-cardiolipina). Uma maneira de estimar a quantidade de anticorpos circulantes é diluir a solução em soro fisiológico até que não haja precipitação mais. Por exemplo: se em 1 ml de solução de plasma e extrato de coração de boi houve precipitação, metade desse volume é diluído em soro fisiológico e analisado de novo. Caso desta vez não haja precipitação, consideramos a titulação como 1/2 (foi preciso diluir metade do volume para que a mistura deixasse de precipitar). Não raro, é necessário diluir muitas e muitas vezes a mistura para que ela deixe de precipitar, rendendo resultados como 1/16, 1/32, 1/64, 1/128... Uma titulação de 1/128 significa que havia uma concentração tão alta de anticorpos que foi preciso diluir 1/128 avos da solução original em soro fisiológico para que ela deixasse de precipitar. Por mais que às vezes seja um pouco trabalhosa e nem sempre precisa (às vezes o técnico de laboratório pode ficar na dúvida se houve precipitação ou não), a técnica do VDRL depende de poucos recursos e pode ajudar bastante a avaliar se um paciente com sífilis está respondendo bem ao tratamento, por exemplo. Principalmente porque testes baseados em anticorpos mais específicos (chamamos de testes treponêmicos, sendo o principal deles o FTA-ABS) continuam positivos para o resto da vida mesmo após o tratamento, de forma que impossível saber se um indivíduo que teve sífilis no passado e foi tratado está novamente com a doença. Com o VDRL, no entanto, embora o paciente que foi tratado corretamente e curado possa permanecer para sempre com uma titulação de 1/2, por exemplo, se seis meses depois ele aparecer com um novo exame indicando uma titulação de VDRL de 1/16, podemos seguramente afirmar que ele adquiriu sífilis novamente.
Não se adquire sífilis apenas por via sexual, embora essa seja a principal forma de transmissão. O motivo pelo qual o VDRL está entre os exames que devem ser pedidos mais de uma vez durante o pré-natal é que o treponema pode atravessar a placenta e chegar ao feto, especialmente no final da gestação. No organismo que está se formando, a sífilis pode acometer o periósteo, a camada de colágeno que reveste os ossos, e causar deformidades ósseas e alterações articulares. Pernas curvas ("tíbia em sabre"), deformidade nasal ("nariz em sela") e anomalias dentárias (dentes de Hutchinson) são descrições clássicas, além de lesões na pele que também são cheias de treponemas, quase como se fossem cancros duros congênitos. Não é raro que também nasçam com anemia, baço aumentado e icterícia (deposição do pigmento biliar resultando em pele amarelada). Se não tratada, a sífilis congênita pode deixar sequelas para toda a vida.
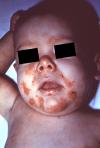
Um recém-nascido com sífilis congênita. Repare nas lesões de pele e no nariz em sela.

Retrato do artista Gerard de Lairesse pelo colega Rembrandt (por volta de 1665). Vítima da sífilis congênita (que posteriormente o cegou), Lairesse tinha alterações faciais típicas da síndrome - repare nos olhos distantes um do outro, na testa proeminente e no nariz em sela.
Existe muita controvérsia sobre a origem da sífilis. Há quem diga que ela sempre circulou na Europa, na Ásia e na África, e passou séculos sendo considerada como uma entidade ligada a outras doenças, como a hanseníase. No entanto, até hoje não se encontrou nenhum esqueleto na Europa que tenha alterações ósseas que permitam concluir com certeza que tal indivíduo tinha sífilis. A teoria mais aceita atualmente indica que, ou a sífilis surgiu na América e foi levada para a Europa após a primeira viagem de Cristóvão Colombo, ou ela surgiu a partir de uma cepa particularmente virulenta de alguma outra doença treponêmica da África e de lá chegou à Europa. De fato, existem algumas regiões da África onde há uma doença parecida com a sífilis chamada bejel, também causada por um subtipo de Treponema pallidum, mas sem transmissão sexual. Em algumas regiões das Américas há outra doença endêmica causada por uma variedade de Treponema pallidum, a pinta, que é transmitida por contato direto com as lesões e não por intercurso sexual. E em ambos os continentes, América e África, assim como na Ásia, há uma terceira doença chamada bouba, causada por outro subtipo de treponema. Tudo indica que, quando os europeus começaram a se aventurar pelos mares e chegar a outros continentes, chegando à África e à América, contraíram sífilis e a levaram para a Europa. Esqueletos com deformidades e reação periosteais datados de mais de 7 mil anos encontrados no continente americano e análises comparativas de DNA sugerem que a sífilis tenha realmente surgido na América. O fato de ser uma doença de transmissão sexual e ter sido levada da América para a Europa em 1492 diz bastante sobre as relações entre europeus e povos nativos.

Uma estatueta peruana do século VI. Alguns afirmam que o nariz em sela e as deformidades dentárias da mãe sugerem tratar-se de sífilis congênita.
A primeira epidemia de sífilis registrada na Europa data de 1495, apenas três anos depois da primeira viagem de Colombo à América. Em 1489, o rei Ferdinando de Nápoles se negou a pagar as dívidas que tinha com o Papa Inocêncio VIII. Após a morte de Ferdinando, seu filho Afonso II ameaçou invadir o ducado de Milão, no norte da Itália. O príncipe de Milão, Ludovico Sforza, apelou para o Papa tentando evitar que seu ducado fosse invadido pelos napolitanos. O Papa, com o objetivo de atender ao apelo de Ludovico, "convidou" o rei da França, Charles VIII, a invadir Nápoles, já que o rei francês considerava ser herdeiro do trono napolitano por alguma árvore genealógica obscura. Essa era uma época em que a Itália estava bastante dividida, com os napolitanos no sul, os venezianos, florentinos e milaneses no norte e os territórios do Papa no meio, além de uma miríade de outras cidades-estados independentes. Como se não bastasse, potências militares ao redor ameaçavam a península constantemente - os franceses no norte, os espanhóis no sul (que também acreditavam ter direito ao trono de Nápoles, como se o reino fosse uma pizza napolitana pronta para ser dividida), e principalmente os turcos otomanos vindo do leste. Foi nessa época conturbada, ainda que mais rica em florescimento cultural com o Renascimento, que Maquiavel escreveu sua obra O Príncipe com o objetivo de aconselhar um governante (no caso algum dos Médici em Florença) a unificar a Itália e impedir que caísse nas mãos de alguma potência estrangeira.
Tentando consolidar seu poder e sua influência sobre Nápoles (e por extensão sobre a Itália), Charles VIII invadiu a Itália com 25 mil soldados, incluindo mercenários suíços, italianos e espanhóis. Inicialmente os italianos do norte aplaudiram a chegada dos franceses porque isso os livraria da ameaça do poderoso reino de Nápoles no sul, mas meses e anos de roubos, depravação e desordem fizeram com que os italianos mudassem de ideia, e o próprio príncipe Ludovico Sforza de Milão se juntou a outros príncipes italianos e acabou por expulsar os franceses. Mas os milaneses contaram com uma ajuda extra: uma epidemia de sífilis se alastrou por entre os soldados franceses, matando, debilitando e enfraquecendo muitos dos soldados que Charles VIII enviara originalmente para conquistar Nápoles. Relatos da época falam de "uma doença de transmissão sexual diferente de todas as que já se havia visto, mais terrível que a lepra, que consistia em erupções generalizadas de pústulas e que podia ser fatal". A agressividade da doença chama a atenção e é mais um ponto a favor da teoria de que a sífilis veio do outro lado do Atlântico. Os povos americanos, convivendo com a doença por milhares de anos, haviam sofrido algum tipo de seleção natural e tinham um perfil genético mais resistente à doença, levando a uma forma mais branda. Os europeus, por outro lado, não tinham essa resistência, e por isso sofreram formas muito mais graves. Eventualmente, variedades mais brandas da doença passaram a prevalecer, porque as formas que matam mais devagar são transmitidas por mais tempo.
Ter uma infecção sexualmente transmissível não costumava ser algo muito bom para a reputação naquela época, e ninguém queria admitir que a doença havia sido trazida por eles. Colocar a culpa no inimigo ou no vizinho era muito mais conveniente. Assim, os napolitanos (e os outros italianos, bem como alemães e ingleses) chamavam a sífilis de "doença francesa". Os franceses chamavam de "doença napolitana", os portugueses, holandeses e marroquinos chamavam de "doença espanhola", os russos diziam que era a "doença polonesa" e os turcos otomanos se referiam como "a doença dos cristãos". Um médico parisiense chamado Jean Fernelius usou o termo "peste venérea" (lues venera), e até hoje "lues" é um termo usado para se referir à sífilis. O termo "sífilis", por sua vez, surgiu com o médico e poeta Girolamo Francastoro, que em 1530 escreveu a obra "Sífilo e a Doença Francesa". Sífilo, um pastor a serviço de um rei grego, teria se revoltado contra o deus Apolo. Como punição, Apolo enviou a doença para acometer Sífilo, o rei e seus súditos, deixando-os terrivelmente desfigurados.

Ilustração de um mercenário com lesões de pele causadas pela sífilis (Albrecht Dürer, 1496).
Por muitas e muitas décadas após a primeira epidemia, a sífilis circulou na Europa, na Ásia, na África e nas sociedades coloniais nas Américas, fazendo um grande número de vítimas que incluía gente famosa como Edouard Manet, Charles Baudelaire, Gustave Flaubert, Arthur Schopenhauer e Friedrich Nietzche, entre outros. Há controvérsias sobre Mozart, Beethoven, Paganini e Schubert.
O mundo precisou esperar até a virada do século XIX para o XX, a era de ouro da Microbiologia, para que o responsável pela sífilis fosse identificado. Em 1905, Schaudinn e Hoffmann identificaram a então batizada como Spirocheta pallida (depois Treponema pallidum). Em 1906, Landsteiner desenvolveu a técnica de microscopia de campo escuro, e em 1910 Wassermann começou a utilizar o primeiro teste sorológico.
Por muito tempo, o tratamento da sífilis foi realizado com plantas medicinais como o guaiacum e sais de metais pesados (mercúrio, bismuto e, posteriormente, arsênico). Infelizmente, esses tratamentos eram bem pouco efetivos porque, ou não matavam os treponemas, ou matavam treponemas E TAMBÉM o indivíduo doente (o arsênico é um veneno poderoso, conhecido há muitos e muitos séculos).
Foi só quando um médico escocês chamado Alexander Fleming esqueceu uma placa de cultura de bactérias no fundo da gaveta de seu laboratório ao sair de férias em 1928 que o tratamento da sífilis se tornou realmente efetivo. Ao voltar para o trabalho, descobriu que as placas de cultura haviam mofado, e que por algum motivo havia um halo em torno da mancha de bolor onde as bactérias não cresciam. O estudo desse fungo, Penicillium notatum, deu origem à penicilina, cuja produção em massa aconteceu com a Segunda Guerra Mundial no início dos anos 1940. Por mais que desde então um número enorme de bactérias tenha desenvolvido mecanismos de resistência à penicilina e a outros antibióticos que foram descobertos ou sintetizados depois, a sífilis continua até hoje sensível à substância. De fato, a penicilina até hoje é o tratamento de escolha para a sífilis, sendo a penicilina cristalina reservada para casos de neurossífilis e o Benzetacil (uma formulação de penicilina de liberação lenta suspensa em uma solução oleosa) em dose única ou em aplicações semanais por 3 semanas usada para casos de sífilis primária, secundária e latente que não envolvam o sistema nervoso central.
Nas últimas décadas do século XIX e no início do século XX, diversas teorias sobre a doença, seu causador e seus mecanismos foram propostas, assim como várias terapias experimentais. Um professor de Dermatologia da Universidade de Oslo chamado Caesar Boeck acreditava que o mercúrio usado no tratamento da sífilis era tóxico e atrapalhava a atividade do sistema imunológico, o verdadeiro responsável pela cura. Como resultado, no período entre 1891 e 1910 ele praticamente proibiu o uso de mercúrio no tratamento da sífilis, e os cerca de 2.000 casos de sífilis em homens brancos adultos atendidos no período ficaram sem receber o tratamento baseado no metal. O sucessor de Boeck, Edvin Bruusgaard, decidiu realizar um estudo retrospectivo para avaliar o que havia acontecido com aquelas pessoas. Seus resultados foram publicados em 1928 e mostraram que havia uma chance de 30 a 40% de um indivíduo não tratado apresentar sífilis terciária, aproximadamente.
O estudo de Bruusgaard foi muito bem recebido nos EUA, e seguindo as teorias racistas da época, um grupo de pesquisadores decidiu fazer um estudo para avaliar se a sífilis evoluiria da mesma forma em homens negros, que tinham uma prevalência elevada da doença. Um estudo prospectivo, que acompanharia pacientes ao longo de um determinado período e depois, a princípio, ofereceria tratamento - ainda que o tratamento na época fosse composto pelos metais pesados e tóxicos mercúrio, arsênico e bismuto, e tivesse eficácia somente em torno de 30%. O lugar perfeito para conduzir um estudo como esse seria no Instituto Tuskegee, no condado de Macon, Alabama. Assim como em todo o restante do sul dos EUA, o Alabama era pobre e povoado por muitos descendentes de escravos.
Batizado com o nome de uma aldeia dos índios Creek que ficava na mesma área, o Instituto Tuskegee havia sido criado para estimular o desenvolvimento econômico daquela região do sul dos EUA. Dentre suas muitas instalações, possuía um pequeno hospital e um corpo assistencial que incluía médicos e enfermeiros negros, o que facilitaria a aceitação do estudo por parte dos pacientes, em sua maioria lavradores pobres e analfabetos. Aos participantes, seriam oferecidos tratamento médico gratuito, refeições e serviço funerário. Assim, em 1932 eles conseguiram uma coorte de 600 pessoas - 399 casos com sífilis e 201 controles sem a doença.
Embora talvez os idealizadores do estudo estivessem realmente motivados por algum ideal humanista, de realizar um estudo sobre as consequências da sífilis em homens negros e assim contribuir para a sociedade justificando a necessidade de tratamento da população negra, havia uma forte tendência ao paternalismo. Os pacientes eram considerados ignorantes demais para compreender a dimensão e as implicações do estudo, e por isso não seria necessário explicar os procedimentos nem sua finalidade. Os pesquisadores diziam que o propósito do estudo e da coleta dos exames era tratar "sangue ruim", e para convencê-los a se submeter a punções lombares para coleta de líquido cefalorraquidiano, eles diziam que estavam realizando um "tratamento especial".
O plano era realizar uma coleta de exames por 6 a 9 meses e depois iniciar o tratamento, ou pelo menos assim pensava o seu principal idealizador, Taliaferro Clark. No entanto, com a crise de 1929 os EUA entraram em uma grave recessão, e os fundos destinados ao estudo foram cortados. Os pacientes não receberiam tratamento. Clark e Raymond Vonderlehr, um de seus diretores subordinados, decidiram manter o acompanhamento dos pacientes mesmo sem o tratamento para mostrar a necessidade de se tratar a população negra. No entanto, quando Vonderlehr propôs que o estudo continuasse além dos 9 meses, Taliaferro Clark se opôs e acabou por sair. Foi de Vonderlehr a ideia de dizer aos participantes que as punções lombares eram "tratamentos especiais" para conseguir que concordassem em se submeter a elas. O estudo prosseguiu por mais quatro décadas.
Outro colaborador, Oliver Wenger, diretor da clínica de doenças venéreas de Hot Springs, Arkansas, estabeleceu os protocolos iniciais para a pesquisa. Embora defendesse que os participantes devessem ser tratados, continuou a colaborar mesmo quando informado que não haveria tratamento, apenas exames. Também defendeu que o verdadeiro propósito do estudo, o acompanhamento da sífilis, não deveria ser informado aos pacientes, pois isso poderia afastá-los ou dificultar sua cooperação.
A equipe de funcionários locais do Instituto Tuskegee continuou a colaborar com os pesquisadores. O fato de ser em sua maioria negros e de conhecer a população local fez com que eles fossem cruciais para que se mantivesse um seguimento e uma boa relação entre os pesquisadores e os pacientes. Os profissionais que mais se destacaram foram o médico Eugene Dibble e Eunice Rivers. O quanto eles sabiam sobre o propósito do estudo de não tratar os pacientes permanece um mistério até hoje. Entre 1947 e 1962, 127 estudantes de Medicina negros se revezaram em atividades ligadas ao estudo no Instituto Tuskegee, inclusive como parte da formação médica.
Em 1936, um dos primeiros trabalhos realizados a partir do estudo de Tuskegee foi criticado por não haver menção a tratamento, e mesmo assim a equipe de pesquisadores reforçou aos colaboradores do Instituto Tuskegee a necessidade de manter o acompanhamento sem que os pacientes fossem tratados. Definiu-se que eles seriam acompanhados até morrer.
Com a eclosão da Segunda Guerra Mundial em 1939, a produção de penicilina precisou ser realizada em larga escala para atender aos muitos feridos em batalha e evitar que morressem de infecção. Os EUA conseguiram isso em 1942. A partir de então, a penicilina passou a ser usada para um enorme número de infecções, e em 1945 ela é considerada a droga de escolha para o tratamento da sífilis. Ou seja, o estudo de Tuskegee prosseguia acompanhando centenas de pessoas com sífilis sem que nenhuma fosse tratada, mesmo com uma recomendação recente de que sim, havia um novo tratamento disponível para a doença e ele era bem mais efetivo e seguro do que os antigos tratamentos com metais pesados.
Quando a guerra acabou e os crimes dos nazistas foram expostos no Tribunal de Nuremberg em 1948, houve comoção mundial com os experimentos médicos realizados por Josef Mengele e outros (que envolviam submeter judeus a condições físicas extremas para descobrir até onde conseguiam sobreviver, ou amputar membros de um indivíduo e reimplantá-lo em seu irmão gêmeo, entre outros). Horrorizados, pesquisadores do mundo inteiro passaram a reavaliar suas condutas éticas e considerar a segurança, a privacidade e o consentimento dos pacientes antes de se iniciar um estudo. E ao mesmo tempo, no Alabama, um estudo que seguia na contramão da História continuava a ser realizado.

Pesquisadores coletam sangue de um dos participantes do estudo de Tuskegee.
Nas décadas seguintes, campanhas de "centros de tratamento rápido" foram estabelecidas em todo o país, inclusive no sul dos EUA, fazendo a prevalência da sífilis cair para bem abaixo dos vergonhosos 35% da década de 1930, quando o estudo começou. Apesar da existência dessas campanhas, os pesquisadores do estudo de Tuskegee fizeram de tudo para evitar que os pacientes recebessem esse tratamento oferecido pelas campanhas, por que isso "estragaria o estudo".
Nos anos 1960, denúncias sobre a ética por trás do estudo de Tuskegee começaram a aparecer. Um jovem médico chamado Irwin Schatz fez a primeira denúncia, que não deu em nada. Mas no ano seguinte um investigador de São Francisco chamado Peter Buxtun encaminhou uma carta ao diretor nacional da Divisão de Doenças Venéreas e a repercussão foi maior. Comparações com os estudos conduzidos pelos nazistas eram inevitáveis. Poucos anos antes, o movimento pelos direitos civis dos negros havia começado a ganhar força, encabeçado por Martin Luther King. Embora o CDC tenha saído em defesa do estudo e afirmado a necessidade de se conduzi-lo até o fim (ou seja, até que todos os participantes morressem e fossem autopsiados), uma comissão do governo dos EUA foi organizada para investigar o caso e concluiu que o estudo de Tuskegee não era justificado eticamente. Ou seja, os benefícios em conhecimento não compensavam os riscos de se privar os pacientes de receber o tratamento adequado. Quando o estudo foi interrompido, no final de 1972, 74 dos 399 pacientes iniciais estavam vivos. 28 haviam morrido de sífilis e 100 morreram de complicações relacionadas. Mas eles não foram as únicas vítimas. As esposas de 40 deles contraíram sífilis, e 19 crianças nasceram com sífilis congênita. Nenhuma dessas mulheres e crianças teria tido a doença se a penicilina tivesse sido administrada aos participantes. Após uma batalha judicial, o governo dos EUA concordou em pagar uma indenização de 10 milhões de dólares para as famílias dos que participaram do estudo, e oferecer tratamento médico e auxílio funerário a todos os 74 que ainda estavam vivos.
O escândalo do estudo de Tuskegee reforçou ainda mais a necessidade de se obter consentimento e de se explicar aos participantes de um estudo a necessidade de cada procedimento ou mesmo a finalidade do estudo em si. Desde então, todo e qualquer pesquisador que se propõe a realizar um estudo precisa preencher uma série de pré-requisitos para não cometer infrações éticas. Entre elas, precisa garantir que o grupo controle, contra o qual está sendo comparada a intervenção que o estudo propõe, precisa receber o tratamento mais efetivo disponível. Dessa forma, se um novo remédio ou procedimento está sendo testado, ele precisa pelo menos não ser pior que o tratamento padrão. Isso hoje nos parece óbvio, mas esta triste história prova que não era para aqueles pesquisadores dos anos 1930.
O fantasma de Tuskegee ainda paira. Na década de 1980, quando a epidemia de AIDS ganhou os noticiários, a desconfiança da população geral para com os órgãos governamentais causada pelo experimento de Tuskegee gerou até mesmo teorias conspiratórias de que a AIDS havia sido desenvolvida para controlar a população mais pobre.
O fantasma de Tuskegee ainda paira. Na década de 1980, quando a epidemia de AIDS ganhou os noticiários, a desconfiança da população geral para com os órgãos governamentais causada pelo experimento de Tuskegee gerou até mesmo teorias conspiratórias de que a AIDS havia sido desenvolvida para controlar a população mais pobre.
A História da sífilis mudou com a epidemia da AIDS. Descobriu-de que as alterações na imunidade causadas pelo HIV fazem com que a sífilis evolua de forma diferente nos indivíduos HIV +, mesmo naqueles que não preenchem critérios para AIDS. As três fases da sífilis podem se seguir em um intervalo menor ou até mesmo coexistir, e a doença parece evoluir mais rápido. Novos desafios se impõem em nossos dias. Uma doença que estava controlada nos anos 1990 voltou com força total nas primeiras décadas do século XXI, e esse parece ser um fenômeno mundial. No Brasil, segundo dados do Ministério da Saúde, entre 2010 e 2016 a taxa de detecção da sífilis adquirida saltou de 2 para cada 100.000 habitantes para 42 para cada 100.000 habitantes, um aumento de mais de 20 vezes em 6 anos. Dentre as gestantes, foi de 3,5 a cada 100.000 habitantes para 12,4 a cada 100.000 habitantes, um aumento de 3 vezes. Em sua maioria, os novos casos ocorrem na população jovem, e as campanhas para uso de preservativos parecem não surtir mais efeito. Para completar, houve um período entre 2015 e 2016 em que a Penicilina Benzatina desapareceu das prateleiras das farmácias em todo o país, com graves prejuízos para o tratamento e para o controle da doença. Os estoques voltaram ao normal, mas não sabemos se há risco de uma nova escassez ocorrer. E o número de casos de sífilis continua a aumentar, havendo Benzetacil ou não.
A reemergência da sífilis tem apresentado novas questões, e ainda não temos as respostas sobre como controlar essa nova epidemia. O que sabemos, no entanto, é que não importa a maneira que encontremos, ela jamais poderá passar por cima da dignidade e do respeito à pessoa. Que escândalos como o de Tuskegee não se repitam jamais.
Nenhum comentário:
Postar um comentário